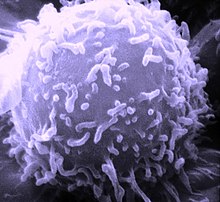
T-lymfocyt
T-lymfocyt (též T-buňka) je druh bílých krvinek ze skupiny lymfocytů. Při růstu opouštějí kostní dřeň a migrují do brzlíku, ve kterém dozrávají. Existuje více typů T-lymfocytů. Obecně se však dá říci, že jsou podstatou specifické (získané) buněčné imunity, při níž potírají např. nádorové buňky či buňky napadené viry. Dále jsou některé T-lymfocyty schopné účinně regulovat imunitní systém – zejména díky tomu, že vylučují do krve cytokiny. Na povrchu T-buněk se nachází mimo jiné tzv. T-buněčný receptor a další markery (zejména CD3, dále CD8 nebo CD4).[1]

Podtypy
editovatExistují dva základní druhy, rozlišované na základě CD markerů na povrchu:
- TH lymfocyt – pomocný T-lymfocyt, který cytokiny stimuluje imunitní reakci; dělí se především na TH1 lymfocyty („zánětové“ TH buňky, schopné i přímé aktivity) a TH2 lymfocyty (typičtí regulátoři, aktivují B-lymfocyty)
- TC lymfocyt – cytotoxický T-lymfocyt, ničí buňky napadené viry a jinými parazity a nádorové buňky; často pomocí interakce mezi FasL a FasR, což vyvolává buněčnou smrt cílových buněk
Oba tyto typy se mohou po proběhnutí primární imunitní odpovědi uchovávat v těle jako paměťové T-lymfocyty. Mimo tyto dva základní druhy byly navrženy další podtypy T-lymfocytů, které jsou vzácné nebo se jejich existence nepotvrdila:
- Treg lymfocyt (regulační T-lymfocyt, někdy též Ts - supresorové) – regulují TH- a B-lymfocyty
- NK T-lymfocyt – podobající se NK buňkám, ale mají i vlastnosti T-buněk[1]
- γδ T-lymfocyt – mnohostranně účinkující T-buňka se zvláštním druhem T-buněčných receptorů na povrchu.[2]
Regulace aktivit TH1 a TH2
editovatO tom, či se budou prekurzorové CD4+ TH buňky vyvíjet směrem k TH1 nebo TH2, rozhoduje poměr dvou cytokinů, které se jmenují IL-12 a IL-4. Cytokin IL-12 je produkován makrofágy a dendritickými buňkami, které jsou stimulované některými mikroorganismy. Naproti tomu cytokin IL-4 je produkován bazofily a mastocyty. Když začne celý proces u makrofágů, bude produkován IL-12 a ten bude stimulovat tvorbu TH1. Začne-li proces probíhat u bazofilů nebo mastocytů, bude produkován především IL-4 a ten bude stimulovat vznik TH2. Cytokiny produkované TH1 buňkami (především IFN-γ) dále podporují vývoj TH1 a silně inhibují vývoj TH2. Naopak IL-4 a IL-10, které jsou produkty TH2, podporují vznik TH2 a inhibují vývoj TH1.[3]
Imunitní reakce založené na cytotoxických T-lymfocytech
editovatCytotoxické T lymfocyty (Tc) jsou důležitými složkami imunitního systému. Jejich úkolem je rozeznat buňky infikované viry nebo jinými intracelulárními parazity, popřípadě jiné poškozené/abnormální buňky (například buňky poškozené stresem či nádorové buňky). Tyto buňky jsou ničeny mechanismy závislými na bezprostředním těsném kontaktu mezi Tc a napadenou buňkou. Způsob obrany je tedy velmi radikální a do značné míry i riskantní, protože poškození tkání cytotoxickými T-lymfocyty může být často mnohem horší než poškození virem, který způsobil infekci.
Zahájení imunitní odpovědi založené na cytotoxických T-lymfocytech probíhá následovně: prekurzor Tc musí rozeznat MHC gp I s antigenními peptidy (např. fragmenty virových proteinů) na povrchu buněk prezentujících antigen (APC). Tyto buňky musí mít patřičně adhezívní molekuly a kostimulační molekuly (CD80, CD86, ligandy receptorů CD28). Takovými APC mohu být dendritické buňky nebo makrofágy. Buňky jsou virem infikovány, nebo pohltí příslušné antigeny, které pocházejí z odumřelých infikovaných, nádorových, či stresových buněk. Když prekurzorová Tc buňka rozezná antigen na povrchu jiných buněk, které nemají stimulační vlastnosti profesionálních APC, dostane pouze první signál a to ji utlumí. Když dojde k prvnímu kontaktu na povrchu účinné APC, prekurzor Tc se začne dělit (proliferovat) a diferencovat na klon zralých efektorových cytotoxických buněk (Tc, CTL).[3]
Aktivace T-lymfocytů superantigenem
editovatJako superantigeny označujeme proteiny, které mají dvě vazebná místa s odlišnou funkcí. Jedním vazebným místem interagují s epitopem přítomným na všech molekulách MHC gp II a tím druhým se strukturami sdílenými mnoha různými molekulami TCR receptoru (těmi, které používají strukturně podobné variabilní úseky). Takový superantigen může propojit MHC gp II na povrchu jakýchkoli antigen prezentující buňky s TCR přítomných na velké části T-lymfocytů. A právě tento krok dá T-lymfocytu signál podobný „normálnímu“ signálu přes TCR, který vede k rychlé aktivaci mnoha T-buněk současně a zároveň k sekreci velkého množství cytokinů, které pak mohou způsobit šokové stavy. Podobné aktivační účinky mají i některé mitogenní lektiny, jako například ConA a nebo PHA. Polyklonální aktivace T-lymfocytů lze také dosáhnout protilátkami proti TCR a nebo CD3.[3]
Protilátková reakce vyvolaná antigeny závislými na T-lymfocytech
editovatSpecifikem protilátkových reakcí vyvolaných antigeny závislými na T-lymfocytech je, že probíhají ve dvou fázích, a to ve fázi primární a sekundární odpovědi. Tyto fáze mohou být jasně oddělené. Závisí to na dávce antigenu a způsobu jeho podávaní. Například když jsou podávány opakované malé dávky s vhodným časovým odstupem. V případe přirozené infekce, kdy v organismu přetrvává, tedy vzniká relativně velké množství antigenu po delší dobu, naopak nebude primární fáze od sekundární oddělená, ale budou na sebe bezprostředně navazovat.[3]
Vyčerpání T buněk
editovatT buněčné vyčerpání se projevuje nesprávnou funkcí T buněk. Vyčerpání je charakterizováno postupnou ztrátou funkce, změnami v transkripčním profilu a dlouhotrvající expresí inhibičních receptorů. Nejprve buňky přichází o schopnost produkce IL-2 a TNF-α následuje ztráta vysoké proliferační kapacity a cytotoxicity. V pozdějším stádiu vyčerpání mohou být T buňky deletovány. Vyčerpané T buňky mají typicky vysoké hladiny CD43, CD69 a inhibičních receptorů naopak snížena je exprese CD62L a CD127. Vyčerpání se může rozvinout během chronické infekce, sepse nebo rakoviny.[4] Vyčerpané T buňky si zachovávají svou změněnou funkčnost i po opakovaném setkání s antigenem.[5]
Vyčerpání během infekce a sepse
editovatVyčerpání může být spuštěno celou řadou faktorů jako je například přetrvávající vystavení antigenu a ztráta pomoci od CD4 T buněk.[6] Vystavení antigenu má také efekt na průběh vyčerpání, jelikož delší vystavení nebo vyšší množství antigenu má za následek zhoršení vyčerpání. Pro rozvinutí vyčerpání je třeba kontinuální vystavení antigenu po dobu alespoň 2-4 týdnů.[7] Dalším faktorem schopným vyvolat vyčerpání jsou inhibiční receptory jako protein PD1, CTLA-4, TIM-3 nebo LAG3.[8][9] Rozpustné molekuly jako jsou cytokiny IL-10 a TGF-β mohou také vyvolat vyčerpání.[10][11] Posledním známým mechanismem vyvolání vyčerpání jsou regulační T buňky. Ty mohou být zdrojem již zmiňovaných cytokinů a mohou proto hrát roli ve spuštění vyčerpání.[12] Kromě toho bylo ukázáno, že po odstranění Treg a blokaci PD1 dochází k neutralizaci vyčerpání.[13] Vyčerpání T buněk se také může objevit během sepse, jako následek cytokinové bouře. Po prvotní fázi sepse dojde k produkci protizánětlivých cytokinů a pro-apoptotických proteinů, aby nedošlo k poškození těla. V tomto prostředí dochází k rozvoji vyčerpání.[14][15] V nedávné době vyšlo několik studií, které nastínily možnost využití blokace inhibičních receptorů v boji se sepsí.[16][17][18]
Vyčerpání během transplantace
editovatBěhem infekce se vyčerpání rozvíjí díky dlouhodobému vystavení antigenu, podobná situace nastává i po transplantaci v případě antigenů ze štěpu.[19] Bylo ukázáno, že reakce T buněk proti štěpu, v případě transplantace ledvin, se v průběhu času zeslabuje.[20] Tyto data ukazují, že vyčerpání T buněk hraje důležitou roli v toleranci štěpu díky deleci aloreaktivních CD8 T lymfocytů.[15][21] Několik studií dále ukázalo pozitivní vliv chronické infekce na přijetí štěpu a jeho dlouhodobé přetrvání právě vlivem vyčerpání T buněk.[22][23][24] I přes existenci dat ukazujících na pozitivní vliv T buněčného vyčerpání během transplantace existují nevýhody. Mezi tyto nevýhody by se dalo počítat například zvýšené množství infekcí nebo náchylnost ke vzniku nádoru.[25]
Vyčerpání během rakoviny
editovatBěhem rakoviny hraje vyčerpání T buněk roli v ochraně nádoru. Podle výzkumu jsou některé buňky s nádorem spojené, ale i samotné buňky nádoru, schopny aktivně indukovat vyčerpání T buněk.[26][27] Vyčerpání může také hrát roli v případě relapsů, jak bylo ukázáno například na případu leukémie.[28] Jedna studie dokonce předložila důkazy o možném využití exprese blokačních receptorů PD-1 a TIM-3 na T buňkách pro odhad pravděpodobnosti relapsu u leukémie.[29] V posledních letech probíhá mnoho experimentů a klinických studií s blokátory inhibičních receptorů a jejich možného využití při léčbě rakoviny. Některé z nich byly uznány jako fungující a jsou nyní jednou z možností terapie pro některé druhy nádorů.[30] Inhibiční receptory cílené těmito léčivy jsou důležité během vzniku a udržení vyčerpání T buněk a jejich zablokování má za následek obnovení funkcí vyčerpaných T buněk.[31]
Reference
editovat- ↑ a b FERENČÍK, M; ROVENSKÝ, J; SHOENFELD, Y; MAŤHA, V. Imunitní systém; informace pro každého. 1. české. vyd. Praha: Grada Publishing, 2005.
- ↑ Archivovaná kopie. www.tcells.org [online]. [cit. 2009-12-21]. Dostupné v archivu pořízeném dne 2009-12-12.
- ↑ a b c d HOŘEJŠÍ, Václav, Jiřina Bartůňková Základy imunologie: Triton, 2009,S.146,ISBN 978-80-7387-280-9
- ↑ YI, John S.; COX, Maureen A.; ZAJAC, Allan J. T-cell exhaustion: characteristics, causes and conversion. Immunology. 2010-02-23, roč. 129, čís. 4, s. 474–481. Dostupné online [cit. 2018-09-23]. ISSN 0019-2805. doi:10.1111/j.1365-2567.2010.03255.x. PMID 20201977. (anglicky)
- ↑ WANG, Qin; PAN, Wen; LIU, Yanan. Hepatitis B Virus-Specific CD8+ T Cells Maintain Functional Exhaustion after Antigen Reexposure in an Acute Activation Immune Environment. Frontiers in Immunology. 2018, roč. 9. Dostupné online [cit. 2018-09-23]. ISSN 1664-3224. doi:10.3389/fimmu.2018.00219. PMID 29483916. (English)
- ↑ MATLOUBIAN, M.; CONCEPCION, R. J.; AHMED, R. CD4+ T cells are required to sustain CD8+ cytotoxic T-cell responses during chronic viral infection. Journal of Virology. 1994-12, roč. 68, čís. 12, s. 8056–8063. PMID: 7966595 PMCID: PMC237269. Dostupné online [cit. 2018-09-23]. ISSN 0022-538X. PMID 7966595.
- ↑ ANGELOSANTO, Jill M.; BLACKBURN, Shawn D.; CRAWFORD, Alison. Progressive Loss of Memory T Cell Potential and Commitment to Exhaustion during Chronic Viral Infection. Journal of Virology. 2012-08-01, roč. 86, čís. 15, s. 8161–8170. PMID: 22623779. Dostupné online [cit. 2018-09-23]. ISSN 0022-538X. doi:10.1128/JVI.00889-12. PMID 22623779. (anglicky) Archivováno 23. 9. 2018 na Wayback Machine.
- ↑ WHERRY, E John. T cell exhaustion. Nature Immunology. 2011-06, roč. 12, čís. 6, s. 492–499. Dostupné online [cit. 2018-09-23]. ISSN 1529-2908. doi:10.1038/ni.2035. (En)
- ↑ OKAGAWA, Tomohiro; KONNAI, Satoru; NISHIMORI, Asami. Cooperation of PD-1 and LAG-3 in the exhaustion of CD4+ and CD8+ T cells during bovine leukemia virus infection. Veterinary Research. 2018-06-19, roč. 49, čís. 1. Dostupné online [cit. 2018-09-23]. ISSN 1297-9716. doi:10.1186/s13567-018-0543-9. PMID 29914540. (En)
- ↑ BROOKS, David G; TRIFILO, Matthew J; EDELMANN, Kurt H. Interleukin-10 determines viral clearance or persistence in vivo. Nature Medicine. 2006-10-15, roč. 12, čís. 11, s. 1301–1309. Dostupné online [cit. 2018-09-23]. ISSN 1078-8956. doi:10.1038/nm1492. PMID 17041596. (En)
- ↑ TINOCO, Roberto; ALCALDE, Victor; YANG, Yating. Cell-Intrinsic Transforming Growth Factor-β Signaling Mediates Virus-Specific CD8+ T Cell Deletion and Viral Persistence In Vivo. Immunity. 2009-07, roč. 31, čís. 1, s. 145–157. Dostupné online [cit. 2018-09-23]. ISSN 1074-7613. doi:10.1016/j.immuni.2009.06.015. PMID 19604493.
- ↑ VEIGA-PARGA, Tamara; SEHRAWAT, Sharvan; ROUSE, Barry T. Role of regulatory T cells during virus infection. Immunological Reviews. 2013-08-15, roč. 255, čís. 1, s. 182–196. Dostupné online [cit. 2018-09-23]. ISSN 0105-2896. doi:10.1111/imr.12085. PMID 23947355. (anglicky)
- ↑ PENALOZA-MACMASTER, Pablo; KAMPHORST, Alice O.; WIELAND, Andreas. Interplay between regulatory T cells and PD-1 in modulating T cell exhaustion and viral control during chronic LCMV infection. Journal of Experimental Medicine. 2014-08-25, roč. 211, čís. 9, s. 1905–1918. PMID: 25113973. Dostupné online [cit. 2018-09-23]. ISSN 0022-1007. doi:10.1084/jem.20132577. PMID 25113973. (anglicky)
- ↑ OTTO, Gordon P; SOSSDORF, Maik; CLAUS, Ralf A. The late phase of sepsis is characterized by an increased microbiological burden and death rate. Critical Care. 2011, roč. 15, čís. 4, s. R183. Dostupné online [cit. 2018-09-23]. ISSN 1364-8535. doi:10.1186/cc10332. PMID 21798063. (En)
- ↑ a b BOOMER, Jonathan S.; TO, Kathleen; CHANG, Kathy C. Immunosuppression in Patients Who Die of Sepsis and Multiple Organ Failure. JAMA. 2011-12-21, roč. 306, čís. 23, s. 2594. Dostupné online [cit. 2018-09-23]. ISSN 0098-7484. doi:10.1001/jama.2011.1829. PMID 22187279. (anglicky)
- ↑ SHINDO, Yuichiro; MCDONOUGH, Jacquelyn S.; CHANG, Katherine C. Anti-PD-L1 peptide improves survival in sepsis. Journal of Surgical Research. 2017-02, roč. 208, s. 33–39. Dostupné online [cit. 2018-09-23]. ISSN 0022-4804. doi:10.1016/j.jss.2016.08.099. PMID 27993215.
- ↑ PATERA, Andriani C.; DREWRY, Anne M.; CHANG, Katherine. Frontline Science: Defects in immune function in patients with sepsis are associated with PD-1 or PD-L1 expression and can be restored by antibodies targeting PD-1 or PD-L1. Journal of Leukocyte Biology. 2016-09-26, roč. 100, čís. 6, s. 1239–1254. Dostupné online [cit. 2018-09-23]. ISSN 0741-5400. doi:10.1189/jlb.4hi0616-255r. PMID 27671246. (anglicky) Archivováno 25. 7. 2020 na Wayback Machine.
- ↑ WEI, Zhengping; LI, Pingfei; YAO, Yao. Alpha-lactose reverses liver injury via blockade of Tim-3-mediated CD8 apoptosis in sepsis. Clinical Immunology. 2018-07, roč. 192, s. 78–84. Dostupné online [cit. 2018-09-23]. ISSN 1521-6616. doi:10.1016/j.clim.2018.04.010.
- ↑ WELLS, Andrew D.; LI, Xian-Chang; STROM, Terry B. The role of peripheral T–cell deletion in transplantation tolerance. Philosophical Transactions of the Royal Society B: Biological Sciences. 2001-05-29, roč. 356, čís. 1409, s. 617–623. PMID: 11375065. Dostupné online [cit. 2018-09-23]. ISSN 0962-8436. doi:10.1098/rstb.2001.0845. PMID 11375065. (anglicky)
- ↑ HALLORAN, Philip F.; CHANG, Jessica; FAMULSKI, Konrad. Disappearance of T Cell-Mediated Rejection Despite Continued Antibody-Mediated Rejection in Late Kidney Transplant Recipients. Journal of the American Society of Nephrology. 2015-07-01, roč. 26, čís. 7, s. 1711–1720. PMID: 25377077. Dostupné online [cit. 2018-09-23]. ISSN 1046-6673. doi:10.1681/ASN.2014060588. PMID 25377077. (anglicky)
- ↑ STEGER, Ulrich; DENECKE, Christian; SAWITZKI, Birgit. Exhaustive Differentiation of Alloreactive CD8+ T Cells: Critical for Determination of Graft Acceptance or Rejection. Transplantation. 2008-05, roč. 85, čís. 9, s. 1339–1347. Dostupné online [cit. 2018-09-23]. ISSN 0041-1337. doi:10.1097/tp.0b013e31816dd64a. (anglicky)
- ↑ MARE-BREDEMEIJER, Emmy L. D. de; SHI, Xiao-lei; MANCHAM, Shanta. Cytomegalovirus-Induced Expression of CD244 after Liver Transplantation Is Associated with CD8+ T Cell Hyporesponsiveness to Alloantigen. The Journal of Immunology. 2015-08-15, roč. 195, čís. 4, s. 1838–1848. PMID: 26170387. Dostupné online [cit. 2018-09-23]. ISSN 0022-1767. doi:10.4049/jimmunol.1500440. PMID 26170387. (anglicky)
- ↑ GASSA, Asmae; JIAN, Fu; KALKAVAN, Halime. IL-10 Induces T Cell Exhaustion During Transplantation of Virus Infected Hearts. Cellular Physiology and Biochemistry. 2016, roč. 38, čís. 3, s. 1171–1181. Dostupné online [cit. 2018-09-23]. ISSN 1015-8987. doi:10.1159/000443067. (english)
- ↑ SHI, X.-L.; DE MARE-BREDEMEIJER, E. L. D.; TAPIRDAMAZ, Ö. CMV Primary Infection Is Associated With Donor-Specific T Cell Hyporesponsiveness and Fewer Late Acute Rejections After Liver Transplantation. American Journal of Transplantation. 2015-05-05, roč. 15, čís. 9, s. 2431–2442. Dostupné online [cit. 2018-09-23]. ISSN 1600-6135. doi:10.1111/ajt.13288. (anglicky)
- ↑ WOO, Seng-Ryong; TURNIS, Meghan E.; GOLDBERG, Monica V. Immune Inhibitory Molecules LAG-3 and PD-1 Synergistically Regulate T-cell Function to Promote Tumoral Immune Escape. Cancer Research. 2012-02-15, roč. 72, čís. 4, s. 917–927. PMID: 22186141. Dostupné online [cit. 2018-09-23]. ISSN 0008-5472. doi:10.1158/0008-5472.CAN-11-1620. PMID 22186141. (anglicky)
- ↑ ZELLE-RIESER, Claudia; THANGAVADIVEL, Shanmugapriya; BIEDERMANN, Rainer. T cells in multiple myeloma display features of exhaustion and senescence at the tumor site. Journal of Hematology & Oncology. 2016-11-03, roč. 9, čís. 1. Dostupné online [cit. 2018-09-23]. ISSN 1756-8722. doi:10.1186/s13045-016-0345-3. PMID 27809856. (En)
- ↑ LAKINS, Matthew A.; GHORANI, Ehsan; MUNIR, Hafsa. Cancer-associated fibroblasts induce antigen-specific deletion of CD8+ T Cells to protect tumour cells. Nature Communications. 2018-03-05, roč. 9, čís. 1. Dostupné online [cit. 2018-09-23]. ISSN 2041-1723. doi:10.1038/s41467-018-03347-0. PMID 29507342. (En)
- ↑ LIU, Long; CHANG, Ying-Jun; XU, Lan-Ping. T cell exhaustion characterized by compromised MHC class I and II restricted cytotoxic activity associates with acute B lymphoblastic leukemia relapse after allogeneic hematopoietic stem cell transplantation. Clinical Immunology. 2018-05, roč. 190, s. 32–40. Dostupné online [cit. 2018-09-23]. ISSN 1521-6616. doi:10.1016/j.clim.2018.02.009.
- ↑ KONG, Y; ZHANG, J; CLAXTON, D F. PD-1hiTIM-3+ T cells associate with and predict leukemia relapse in AML patients post allogeneic stem cell transplantation. Blood Cancer Journal. 2015-07, roč. 5, čís. 7, s. e330–e330. Dostupné online [cit. 2018-09-23]. ISSN 2044-5385. doi:10.1038/bcj.2015.58. PMID 26230954. (En)
- ↑ U.S. FDA Approved Immune-Checkpoint Inhibitors and Immunotherapies. Medical Writer Agency | 香港醫學作家 | MediPR | MediPaper Hong Kong. 2018-08-21. Dostupné online [cit. 2018-09-23]. (anglicky)
- ↑ BHADRA, Rajarshi; GIGLEY, Jason P.; WEISS, Louis M. Control of Toxoplasma reactivation by rescue of dysfunctional CD8+ T-cell response via PD-1–PDL-1 blockade. Proceedings of the National Academy of Sciences. 2011-05-31, roč. 108, čís. 22, s. 9196–9201. PMID: 21576466. Dostupné online [cit. 2018-09-23]. ISSN 0027-8424. doi:10.1073/pnas.1015298108. PMID 21576466. (anglicky)
Externí odkazy
editovat- Obrázky, zvuky či videa k tématu T-lymfocyt na Wikimedia Commons