Ketamin
Ketamin je léčivo používané v humánní i veterinární medicíně jako anestetikum např. pod obchodními názvy Ketanest, Ketaset, Ketalar, Narkamon a Calypsol. Působí jako antagonista NMDA receptorů,[2] ve vysokých, plně anestetických dávkách obsazuje i opioidní receptory a sigma-receptory. Podobně jako fencyklidin (PCP) vyvolává stavy nazývané disociativní anestezie a zhruba od roku 1965 je zneužíván i jako rekreační droga. Kromě anestetického účinku způsobuje halucinace a hypertenzi. Ketamin je chirální sloučenina a často se prodává jako směs obou izomerů (enantiomerů), (S)-ketaminu a (R)-ketaminu.
| Ketamin | |
|---|---|
 | |
| Název (INN) | Ketamine |
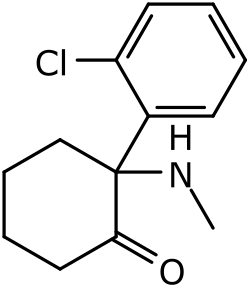
| Název podle IUPAC | (RS)-2-(2-chlorfenyl)-2-(methylamino)cyklohexanon |
| Další názvy | Ketanest, Ketaset, Ketalar |
| Kódy | |
| Číslo CAS | 6740-88-1 |
| Klasifikace ATC | N01AX03 |
| ChEMBL ID | CHEMBL742 |
| ChemSpider ID | 3689 |
| PubChem | 3821 |
| Chemie | |
| Sumární vzorec | C13H16ClNO |
| SMILES | CNC1(CCCCC1=O)C2=CC=CC=C2Cl |
| InChI | InChI=1S/C13H16ClNO/c1-15-13(9-5-4-8-12(13)16)10-6-2-3-7-11(10)14/h2-3,6-7,15H,4-5,8-9H2,1H3 |
| Molární hmotnost | 237,72 g/mol |
| Teplota tání | 262 °C |
| Disociační konstanta | 7,5 |
| Farmakologie | |
| Indikace | bolest a zneužívání návykových látek |
| Metabolismus | játra (CYP3A4[1]) |
| Vylučování | ledvinami (>90 %) |
| Biologický poločas | 2,5–3 hodiny |
| Některá data mohou pocházet z datové položky. | |
Historie
editovatKetamin na začátku 60. let 20. století objevil Calvin Stevens z Wayne State University. V 70. letech už byla látka používána na bojištích války ve Vietnamu, už tam se však začaly objevovat zprávy o zvláštních halucinacích v období, kdy pacienti přicházeli k vědomí.[3] Od 80. let se však ketamin zneužívá jako klubová droga (ač v menším rozsahu než metamfetamin či extáze).[3]
Využití v medicíně
editovatKetamin je disociativní anestetikum. Na rozdíl od ostatních anestetik stimuluje kardiovaskulární i dechové centrum a je potentním analgetikem.[zdroj?] Je to jediné anestetikum používané v humánní medicíně, které zvyšuje krevní tlak. To ho předurčuje pro použití u pacientů, kteří ztratili velké množství krve nebo jsou v šoku. Myorelaxace je slabá, naopak tonus horních cest dýchacích je zachovaný (nedochází k zapadnutí jazyka). Spolehlivého účinku je dosaženo i po nitrosvalovém podání. Účinek nastupuje rapidně, většinou do tří minut po podání, jelikož ketamin je až 10× více liposolubilní než thiopental. Tyto vlastnosti ho předurčuji k použití v medicíně katastrof, protože je bezpečný i v rukou nevyškoleného anesteziologa. Širšímu použití v klinické praxi zabraňují nežádoucí účinky, zejména vysoký výskyt psychických fenoménů – halucinace, děsivé sny, dezorientace, senzorické a percepční iluze. Tyto mají pravděpodobně podklad v redistribuci a pomalém uvolňování ketaminu z tukových tkání (viz tiopental). Lze je zmírnit současným podáním sedativa, např. diazepamu. Mírně zvyšuje nitrolební tlak.
Ketamin se obvykle aplikuje intravenózní nebo intramuskulární injekcí. V humánní medicíně se občas používá jako anestetikum u dětských či naopak starších pacientů (u nichž má zřejmě méně vedlejších účinků než ostatní látky tohoto typu), vždy však v kombinaci se sedativy, aby se zabránilo halucinacím.[3] Zkoumá se také jeho využití při léčbě alkoholismu, závislosti na heroinu, léčbě deprese nebo bolestí.[4][5] Ve veterinární medicíně se ketamin používá hlavně v kombinaci s xylazinem k anestezi nebo analgezi u koček, psů a jiných malých zvířat (90 % ketaminu prodaného legálně v USA jde do veterinárního lékařství[3]).
Rekreační zneužívání
editovatKetamin se zneužívá pro své disociativní účinky podobné účinkům fencyklidinu (PCP) a dextromethorfanu (DXM). Účinek trvá od 45 minut do několika hodin, ale osoba se cítí v pořádku až přibližně za 24–48 hodin. Aplikuje se v této souvislosti injekčně, šňupáním nebo kouřením. Vyvolává ketaminový trip, projevující se např. halucinacemi, pocity depersonalizace, derealizace a oddělení od vlastního těla.[6] Ve vyšších dávkách vede disociace k extrémním stavům typu „k-hole“ až „ego death“, tj. pocit splynutí mysli s okolním světem, např. má člověk pocit, že je nehmotná entita vznášející se vesmírem[zdroj?]. Na rozdíl od jiných látek s halucinogenními účinky (psychedelických tryptaminů a fenylethylaminů[zdroj?]) může vyvolat poměrně silnou psychickou závislost, zvlášť pokud je zneužíván soustavně.[3] Subanestetická dávka má rychlý, ale přechodný antidepresivní efekt, neboť dojde k indukci synaptogeneze přes mTOR a efekt je blokován rapamycinem. John Lilly a David Woodard (mimo jiné) rozsáhle psali o svých vlastních psychonautických zkušenostech s ketaminem.[7]:s.288–295
Dlouhodobé negativní efekty
editovatChronické užívání ketaminu může vést ke zhoršení kognitivních funkcí včetně paměti.[8]
V roce 1989 profesor psychiatrie John Olney publikoval, že ketamin způsobil nezvratné změny ve dvou malých oblastech mozku pokusných krys. Nicméně, zrovna tyto dvě oblasti člověka a krysy se svými metabolickými procesy značně liší, tudíž ten samý proces nemusí u člověka probíhat.[9][10][11]
První širší, dlouhodobá studie uživatelů ketaminu zjistila, že lidé často zneužívající tuto látku (nejméně 4 dny v týdnu a zároveň 20 dní v měsíci) jsou více depresivní a mají zhoršené různé úseky paměti včetně verbální, krátkodobé a vizuální. U méně častých uživatelů ketaminu (užití 4 dny v měsíci) nebyly na poli pozornosti, paměti a psychické pohody zjištěny rozdíly vůči kontrolní skupině. Stejně na tom byli bývalí uživatelé ketaminu. To podporuje názor, že méně časté užívání ketaminu nezpůsobuje kognitivní deficit a že kognitivní deficit u častých uživatelů je vratný při abstinenci. Ovšem bývalí uživatelé, častí i ti méně častí, měli vyšší skóre v testu bludných příznaků než kontrolní skupina.[12]
Užívání ketaminu si, stejně jako u jiných drog, vybírá i oběti na životech. V říjnu 2023 zemřel na předávkování americký herec Matthew Perry.[1]
Odkazy
editovatReference
editovatV tomto článku byl použit překlad textu z článku Ketamine na anglické Wikipedii.
- ↑ HIJAZI, Y.; BOULIEU, R. Contribution of CYP3A4, CYP2B6, and CYP2C9 isoforms to N-demethylation of ketamine in human liver microsomes. Drug Metab Dispos.. 2002, roč. 30, čís. 7, s. 853–8. Dostupné online. ISSN 0090-9556.
- ↑ Harrison N, Simmonds M. Quantitative studies on some antagonists of N-methyl D-aspartate in slices of rat cerebral cortex. Br J Pharmacol. 1985, roč. 84, čís. 2, s. 381–391. Dostupné online. PMID 2858237.
- ↑ a b c d e BIGELOW, Barbara C.; EDGAR, Kathleen J. The UXL Encyclopedia of Drugs & Addictive Substances. [s.l.]: Thomson-Gale, 2006. Dostupné online. ISBN 1-4144-0444-1.
- ↑ Krystal J, Madonick S, Perry E, Gueorguieva R, Brush L, Wray Y, Belger A, D'Souza D. Potentiation of low dose ketamine effects by naltrexone: potential implications for the pharmacotherapy of alcoholism. Neuropsychopharmacology. 2006, roč. 31, čís. 8, s. 1793–800. doi:10.1038/sj.npp.1300994. PMID 16395307.
- ↑ Jovaisa T, Laurinenas G, Vosylius S, Sipylaite J, Badaras R, Ivaskevicius J. Effects of ketamine on precipitated opiate withdrawal. Medicina (Kaunas). 2006, roč. 42, čís. 8, s. 625–634. PMID 16963828.
- ↑ AJ Giannini,N Underwood, M Condon. Acute ketamine intoxication treated by haloperidol.American Journal of Therapeutics. 7:389–743,2000, PMID 11304647.
- ↑ Woodard, D., “The Ketamine Necromance”, v A. Parfrey, Apocalypse Culture II (Los Angeles: Feral House, 2000), str. 288–295. (ang.)
- ↑ Okon T. Ketamine: an introduction for the pain and palliative medicine physician. Pain Physician. 2007, s. 493–500. Dostupné v archivu pořízeném dne 2013-05-22. PMID 17525784. Archivovaná kopie. www.painphysicianjournal.com [online]. [cit. 2013-07-30]. Dostupné v archivu pořízeném z originálu dne 2013-05-22.
- ↑ Olney JW, Labruyere J, Price MT. Pathological changes induced in cerebrocortical neurons by phencyclidine and related drugs. Science. 1989, s. 1360–2. doi:10.1126/science.2660263. PMID 2660263.
- ↑ Erowid DXM Vaults: Health: The Bad News Isn't In: A Look at Dissociative-Induced Brain Damage, by Anderson C
- ↑ Tryba M, Gehling M. Clonidine--a potent analgesic adjuvant. Current Opinion in Anaesthesiology. 2002, s. 511–7. Dostupné online. doi:10.1097/00001503-200210000-00007. PMID 17019247. Archivovaná kopie. meta.wkhealth.com [online]. [cit. 2013-07-30]. Dostupné v archivu pořízeném z originálu dne 2013-05-14.
- ↑ MORGAN, Celia J. A.; MUETZELFELDT, Leslie; CURRAN, H. Valerie. Consequences of chronic ketamine self-administration upon neurocognitive function and psychological wellbeing: a 1-year longitudinal study. Addiction. 2009, s. 121–133. doi:10.1111/j.1360-0443.2009.02761.x. PMID 19919593.
Literatura
editovat- HOLUBOVÁ, Kristína. ŠÓŠ, Peter. REVAYOVÁ, Anna et al. Možnosti modulace antidepresivního účinku ketaminu. Psychiatrie. 2017, roč. 21, č. 1, s. 31–38. ISSN 1211-7579. Dostupné také z: http://www.tigis.cz/casopisy/
- HORÁČEK, Jiří. LIPSKI, Michaela. ŠÓŠ, Peter. Příběh jedné molekuly: čtyři tváře ketaminu. Vesmír. 2016, roč. 95, č. 5, s. 272–275. ISSN 0042-4544.
- HOLUBOVÁ, Kristína. KLETEČKOVÁ, Lenka. ŠKURLOVÁ, Martina. ŘÍČNÝ, Jan. STUCHLÍK, Aleš. VALEŠ, Karel. Rapamycin blocks the antidepressant effect of ketamine in task-dependent manner. Psychopharmacology. 2016, roč. 233, č. 11, s. 2077–2097. DOI: 10.1007/s00213-016-4256-3. ISSN 1432-2072. Dostupné také z: http://www.ncbi.nlm.nih.gov/pubmed/27004790
- KUBEŠOVÁ, Anna. HORÁČEK, Jiří. Vliv psychotropních látek na neurogenezi v dospělém savčím hipokampu. Psychiatrie. 2013, roč. 17, č. 1, s. 19–22. ISSN 1211-7579.
Externí odkazy
editovat- Obrázky, zvuky či videa k tématu ketamin na Wikimedia Commons
- https://web.archive.org/web/20081025015435/http://www.saferparty.cz/ketamin
- http://www.drogypuppy.estranky.cz/clanky/halucinogeny/ketamin
- (anglicky) eMedicine: Ketamine Emergency Applications
- (anglicky) Erowid.org's John C. Lilly Vault
- (anglicky) Club drug finds use as antidepressant – Psychedelic ketamine hits the blues surprisingly fast; Nature.com