Chloristan amonný
Chloristan amonný (AP – z anglického „Ammonium perchlorate") je anorganická sloučenina s chemickým vzorcem NH4ClO4. Je to bezbarvá nebo bílá pevná látka, která je rozpustná ve vodě. Je to silné oxidační činidlo. V kombinaci s palivem může být použit jako raketová pohonná látka pod názvem kompozitní pohonná směs chloristanu amonného. Jeho nestabilita způsobila řadu nehod, jako třeba katastrofu PEPCON.
| Chloristan amonný | |
|---|---|
 Vzorec chloristanu amonného | |
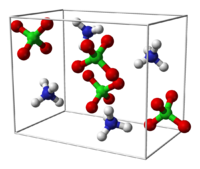 Krystalická struktura | |
 Chloristan amonný | |
| Obecné | |
| Systematický název | Chloristan amonný |
| Ostatní názvy | AP |
| Anglický název | Ammonium perchlorate |
| Německý název | Ammoniumperchlorat |
| Sumární vzorec | NH4ClO4 |
| Vzhled | bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 7790-98-8 |
| EC-no (EINECS/ELINCS/NLP) | 232-235-1 |
| PubChem | 24639 |
| UN kód | 1442 |
| SMILES | [O-]Cl(=O)(=O)=O.[NH4+] |
| InChI | InChI=1S/ClHO4.H3N/c2-1(3,4)5;/h(H,2,3,4,5);1H3 |
| Číslo RTECS | SC7520000 |
| Vlastnosti | |
| Molární hmotnost | 117,49 g/mol |
| Teplota tání | při teplotě >200 °C se rozkládá |
| Hustota | 1,95 g/cm3 (24 °C) |
| Rozpustnost ve vodě | 11,56 g/100 g (0 °C) 20,85 g/100 g (20 °C) 57,01 g/100 g (100 °C) |
| Struktura | |
| Krystalová struktura | Kosočtverečná (<240 °C) Krychlová (>240 °C) |
| Bezpečnost | |
| H-věty | H201, H271, H319, H373 |
| P-věty | P210, P220, P221, P230, P240, P250, P260, P264, P280, P283, P305+P351+P338, P306+P360, P314, P337+P313, P370+P378, P370+P380, P371+P380+P375,P372, P373, P401, P501 |
| NFPA 704 |  0
1
4
OX
|
| Teplota vznícení | 240 °C |
Některá data mohou pocházet z datové položky. | |
Výroba
editovatChloristan amonný (AP) se vyrábí reakcí amoniaku s kyselinou chloristou. Tento proces je hlavním odbytištěm průmyslové výroby kyseliny chloristé. Tato sůl se může vyrábět také podvojnou záměnou amonných solí s chloristanem sodným. Tento proces využívá relativně nízké rozpustnosti NH4ClO4, která činí asi 10 % rozpustnosti chloristanu sodného.[1]
Chloristan amonný krystalizuje v bezbarvé kosočtverečné soustavě.
Rozklad
editovatJako většina amonných solí se chloristan amonný rozloží již před roztavením. Mírné zahřívání vede k rozkladu za vzniku chlorovodíku, dusíku, kyslíku a vody.
- 4 NH4ClO4 → 4 HCl + 2 N2 + 5 O2 + 6 H2O
Spalování AP je poměrně složité a je široce studováno. Krystaly AP se před roztavením rozkládají, i když byla na povrchu krystalů během vysokotlakých spalovacích procesů pozorována tenká vrstva kapaliny.[2] Silné zahřívání může vést k výbuchu. Kompletní reakce nezanechávají žádné zbytky. Čisté krystaly nemohou udržet plamen pod tlakem 2 MPa .
AP je oxidační činidlo 4. třídy (může podstoupit výbušnou reakci) pro částice o velikosti nad 15 mikrometrů[3] a je klasifikováno jako výbušnina pro částice o velikosti menší než 15 mikrometrů.[4][5]
Využití
editovatPrimární využití chloristanu amonného je při výrobě pevných paliv. Když je AP smíchán s palivem (jako práškový hliník a/nebo s elastomerním pojivem), může generovat samočinné spalování při tlacích hluboko pod atmosférickým tlakem. Jedná se o důležité okysličovadlo s desítkami let dlouhou historií použití v raketových motorech na tuhé pohonné látky – kosmické lety (včetně pomocných urychlovacích stupňů raketoplánu Space Shuttle – Solid Rocket Boosters), vojenské, amatérské a hobby High-power rakety a také v některých ohňostrojích.
Některá "rozbitná" epoxidová lepidla obsahují suspenze AP. Při zahřátí nad 300 °C degraduje chloristan amonný organické lepidlo a porušuje tmelený spoj.
Toxicita
editovatChloristany samy o sobě způsobují pouze malou akutní toxicitu. Například chloristan sodný má LD50 2–4 g/kg a po požití se rychle vylučuje.[1] Ukázalo se však, že chronická expozice chloristanům, a to i v nízkých koncentracích, způsobuje různorodé problémy se štítnou žlázou, protože jsou přijímány namísto jódu.
Reference
editovatV tomto článku byl použit překlad textu z článku Ammonium perchlorate na anglické Wikipedii. https://www.europapress.es/economia/noticia-comunicado-perclorato-amonio-web-ammoniumperchlorateorg-20200304141258.html
- ↑ a b Helmut Vogt, Jan Balej, John E. Bennett, Peter Wintzer, Saeed Akbar Sheikh, Patrizio Gallone "Chlorine Oxides and Chlorine Oxygen Acids" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH. doi:10.1002/14356007.a06_483
- ↑ BOGGS, T. L. Deflagration Rate, Surface Structure and Subsurface Profile of Self-Deflagrating Single Crystals of Ammonium Perchlorate. AIAA Journal. 1970, s. 867–873. doi:10.2514/3.5780. Bibcode 1970AIAAJ...8..867B.
- ↑ NFPA 400: Hazardous Materials Code, 2010
- ↑ NFPA 495: Explosive Materials Code, 2010
- ↑ "Development of an Enhanced Hazard Classification System for Oxidizers Research Project, Technical Report", Safety Engineering Laboratories, Inc., The Fire Protection Research Foundation, 13 April 2006
Externí odkazy
editovat- Obrázky, zvuky či videa k tématu chloristan amonný na Wikimedia Commons



