Kyselina trifluoroctová
chemická sloučenina
Kyselina trifluoroctová (TFA) je chemická sloučenina s chemickým vzorcem CF3CO2H. K této karboxylové kyselině jsou navázány tři velmi elektronegativní atomy fluoru. Kyselina je derivátem od kyseliny octové, je přitom téměř stotisíckrát kyselejší. Kyselina je široce používána v organické chemii.[2]
| Kyselina trifluoroctová | |
|---|---|
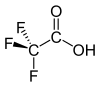 Strukturní vzorec | |
 Molekula | |
| Obecné | |
| Systematický název | trifluorethanová kyselina |
| Ostatní názvy | TFA |
| Funkční vzorec | CF3COOH |
| Sumární vzorec | C2HF3O2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 76-05-1 |
| EC-no (EINECS/ELINCS/NLP) | 200-929-3 |
| Indexové číslo | 607-091-00-1 |
| SMILES | FC(F)(F)C(O)=O |
| Vlastnosti | |
| Molární hmotnost | 114,03 g/mol |
| Teplota tání | −15,4 °C |
| Teplota varu | 72,4 °C |
| Hustota | 1,535 1 g/cm³ (20 °C) |
| Disociační konstanta pKa | 0,3 |
| Rozpustnost ve vodě | mísitelná |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R20 R35 R52/53 |
| S-věty | (S1/2) S9 S26 S27 S28 S45 S61 |
Některá data mohou pocházet z datové položky. | |
Odkazy
editovatReference
editovat- ↑ a b Trifluoroacetic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ LÓPEZ, Simón E.; SALAZAR, José. Trifluoroacetic acid: Uses and recent applications in organic synthesis. Journal of Fluorine Chemistry. Roč. 156, s. 73–100. Dostupné online [cit. 2017-10-20]. DOI 10.1016/j.jfluchem.2013.09.004.
Související články
editovatExterní odkazy
editovat- Obrázky, zvuky či videa k tématu kyselina trifluoroctová na Wikimedia Commons

