Fluorid antimonitý
Fluorid antimonitý, SbF3, je jedním ze dvou fluoridů antimonu, druhým je fluorid antimoničný. Někdy se označuje jako Swartsovo činidlo, protože se využívá jako činidlo ve Swartsově reakci.[1]
| Fluorid antimonitý | |
|---|---|
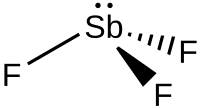 Strukturní vzorec | |
 Krystalová struktura | |
| Obecné | |
| Systematický název | Fluorid antimonitý |
| Anglický název | Antimony trifluoride |
| Německý název | Antimon(III)-fluorid |
| Sumární vzorec | SbF3 |
| Vzhled | světle šedý až bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 7783-56-4 |
| SMILES | F[Sb](F)F |
| InChI | InChI=1S/3FH.Sb/h3*1H;/q;;;+3/p-3 |
| Vlastnosti | |
| Molární hmotnost | 178,76 g/mol |
| Teplota tání | 292 °C |
| Teplota varu | 376 °C |
| Hustota | 4,379 g.cm−3 |
| Rozpustnost ve vodě | 385 g/100 g (0 °C) 443 g/100 g (20 °C) 562 g/100 g (30 °C) |
Některá data mohou pocházet z datové položky. | |
Příprava a struktura
editovatPřipravuje se fluorací oxidu antimonitého fluorovodíkem:
- Sb2O3 + 6 HF → 2 SbF3 + 3 H2O
Je slabou Lewisovou kyselinou, ve vodě pomalu hydrolyzuje.[1] Fluorem se oxiduje na fluorid antimoničný:
- SbF3 + F2 → SbF5
Krystalová struktura je tvořena oktaedry SbF6 propojenými vrcholy (fluoridovými můstky). Tři vazby Sb-F jsou kratší (192 pm) a tři delší (261 pm).[2] Protože má polymerní strukturu je méně těkavý než fluorid arsenitý a chlorid antimonitý.
Využití
editovatSlouží jako fluorační činidlo v organické chemii.[3] Tuto schopnost poprvé popsal belgický chemik Frédéric Swarts v roce 1892. Fluorid antimonitý dokáže fluorovat organické i anorganické chloridy:[1]
- CCl3CCl3 + SbF3 → CCl2FCCl2F
- SiCl4 + SbF3 → SiCl3F, SiCl2F2, SiClF3
Někdy může vystupovat i jako slabé oxidační činidlo:[1]
- 3 PhPCl2 + 4 SbF3 → 3 PhPF4 + 2 Sb + 2 SbCl3
Odkazy
editovatReference
editovatV tomto článku byl použit překlad textu z článku Antimony trifluoride na anglické Wikipedii.
- ↑ a b c d GREENWOOD, N. N.; EARNSHAW, A. Chemie prvků. Sv. 1.. 1. vyd. vyd. Praha: Informatorium, 1993. 793 s., 1 příl s. ISBN 8085427389, ISBN 9788085427387. S. 685–686.
- ↑ EDWARDS, A. J. Fluoride crystal structures. Part XIV. Antimony trifluoride: a redetermination. Journal of the Chemical Society A: Inorganic, Physical, Theoretical. 1970, s. 2751. Dostupné online [cit. 2023-11-17]. ISSN 0022-4944. DOI 10.1039/j19700002751. (anglicky)
- ↑ Kirk-Othmer Encyclopedia of Chemical Technology. Příprava vydání Kirk-Othmer. 1. vyd. [s.l.]: Wiley Dostupné online. ISBN 978-0-471-48494-3, ISBN 978-0-471-23896-6. DOI 10.1002/0471238961.0114200906180505.a01.pub2. (anglicky) DOI: 10.1002/0471238961.
Externí odkazy
editovat- Obrázky, zvuky či videa k tématu fluorid antimonitý na Wikimedia Commons